Proč je voda nepolární rozpouštědlo?
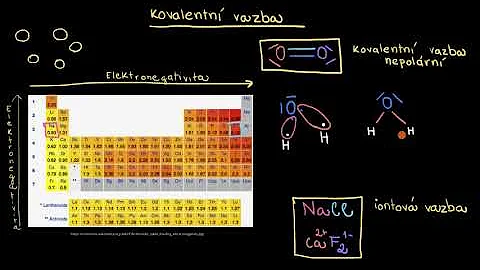
Proč je voda nepolární rozpouštědlo?
Nepolární rozpouštědla rozpustí nepolární molekuly, jako jsou tuky a jiných organických sloučenin. Proč Voda je nazýván Universal Solvent Voda rozpouští více chemikálií, než jakékoliv jiné rozpouštědlo, protože jeho polární povaha dává každému molekuly hydophobic (voda-bát) a hydrofilní (ve vodě) milující stranu.
Co jsou polární rozpouštědla?
Polární rozpouštědla jsou kapaliny, které mají velký dipólový moment. Jedná se o kapaliny, které mohou rozpouštět polární sloučeniny. Je to proto, že jak polární rozpouštědla, tak polární sloučeniny mají dipólové momenty a mají opačně nabité zbytky ve stejné chemické sloučenině.
Co jsou nepolární molekuly?
Nepolární molekuly: Rozdíl elektronegativity mezi atomy je> 0,4. Polární molekuly: Molekulární síly jsou spíše silné a tvoří H-vazby nebo dipólové-dipólové vazby. Nepolární molekuly: Molekulární síly jsou nejslabší dostupné; formy rozptýlené síly v Londýně.
Proč vzniká polarita rozpouštědla?
Polarita rozpouštědla vzniká v důsledku propojení atomů s různými hodnotami elektronegativity za vzniku molekuly. Zde více elektronegativní atom přitahuje vazebné elektronové páry, což nakonec dává méně elektronegativnímu atomu částečný kladný náboj v důsledku snížení hustoty elektronů kolem sebe.














